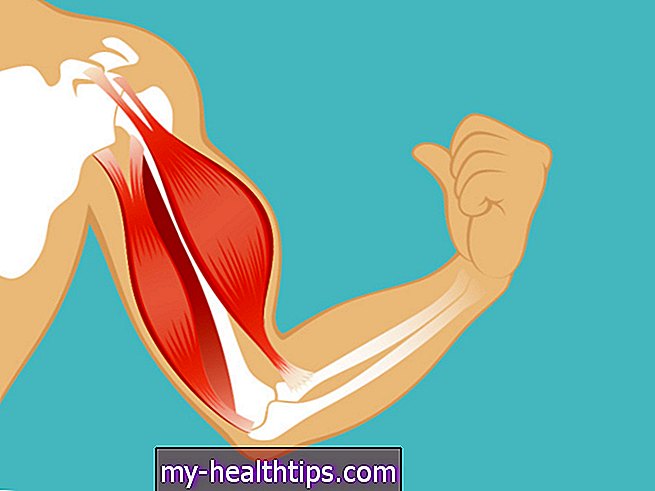
En af de længstlevende virksomheder, der er involveret i diabetesteknologi, er Medtronic Diabetes, som gennem årene har haft en snoet vej i sin produktpipeline.
Virksomheden har været førende inden for insulinpumper, der går tilbage i årtier og var den første til at lancere en kombinationsenhed med en kontinuerlig glukosemonitor (CGM). Som en stærk leder inden for farmaceutisk industri har patienter en tendens til at have et kærlighedshat-forhold til dette firma - værdsætter deres tilbud, men ikke altid deres kundeservice eller marketingtaktik.
Uanset hvordan du skærer det ud, hjælper Medtronic Diabetes med at føre an inden for diabetesteknologi, så det er vigtigt at vide, hvad virksomheden holder på med. Her er et dybt dyk i, hvad Medtronic Diabetes tilbyder i 2020 og derefter:
Nuværende diabetesværktøjer
Fra midten af 2020 er her, hvad Medtronic Diabetes tilbyder med hensyn til tekniske værktøjer:
Minimeret 670G (hybrid lukket sløjfe)
Minimed 670G var en førstegang for vores diabetesfællesskab med denne tidlige hybrid lukkede sløjfe (HCL), der fik Food and Drug Administration (FDA) godkendelse i september 2016.

”Hybrid Closed Loop” betyder egentlig bare, at insulinafgivelsessystemet er delvist automatiseret, men stadig kræver en vis kontrol af brugeren. Den officielle FDA-definition bliver lidt mere teknisk.
Den måde, den fungerer på, er, at CGM-sensoren læser glukosedata hvert 5. minut, og den "lukkede sløjfe" -algoritme, der er indbygget i pumpen, bruger disse oplysninger til at øge eller mindske basal (baggrund) insulinafgivelse for at holde glukoseniveauer så tæt som muligt på en fast mål på 120 mg / dL (til mange brugeres forfærdelse kan dette niveau ikke justeres).
Brugere skal stadig indtaste kulhydratantal og bolusbeløb for at dække måltider og advare systemet på forhånd om enhver øvelse. Det giver heller ikke automatiske korrektionsbolusser baseret på CGM, men det antyder korrektionsbeløb, når et fingersticksglucoseresultat indtastes.
670G blev lanceret i 2017 til høje forventninger, men da den var en tidlig og stadig begrænset “kunstig bugspytkirtel” med nogle klare begrænsninger, blev den ikke så stærk en positiv reaktion fra mennesker med diabetes som virksomheden havde håbet.
Se vores 670G nyhedsdækning og produktanmeldelser for flere detaljer.
Smart insulinpen: Companions InPen
I august 2020 meddelte Medtronic Diabetes, at de erhvervede Companion Medicals opstart og den Bluetooth-aktiverede insulinpen, kendt som InPen. Dette er den eneste FDA-ryddede genanvendelige insulinpen, der forbinder med en app for at spore data og giver brugerne personlige doseringsanbefalinger for kortvirkende insulin (Humalog, Novolog, Fiasp).

Indtil nu har insulinpumper været Medtronics eneste leveringsmetode, der tilbydes patienterne; men nu ved at købe sig ind på markedet for intelligente insulinpenne vil der være en ny mulighed for dem, der vælger injektioner snarere end pumpeterapi.
Medtronic siger, at det ikke planlægger at ændre InPens evne til at oprette forbindelse til CGM'er som Dexcom og Eversense implanterbare CGM, og det planlægger også at oprette forbindelse til Medtronic's Guardian CGM i fremtiden.
Du kan læse vores fulde dækning af Medtronic's InPen-erhvervelse her.
Guardian Connect CGM
Guardian Connect er navnet på Medtronic's enkeltstående CGM-enhed, som har været tilgængelig siden marts 2018 og ikke behøver at blive parret med en insulinpumpe for at arbejde. Guardian Connect var virksomhedens første nye stand-alone CGM-produkt, der blev tilbudt i et årti.

I modsætning til 670G-systemet, der ikke tilbyder nogen deling af data eller fjernovervågning, tilbyder denne enkeltstående CGM indbygget Bluetooth Low Energy til datadeling direkte med en smartphone. Den bruger den samme Guardian 3-sensor, der er godkendt til brug med 670G, og især omgår den behovet for en separat dedikeret modtagerenhed til at se data.
Dette er ikke kalibreringsfrit, hvilket er forskelligt fra konkurrerende CGM-produkter (Dexcom G5- og G6-versioner og FreeStyle Libre), der ikke kræver fingeraftrykbekræftelse inden nogen behandling eller insulindosering. Det er også kun godkendt til brug i alderen 14 år og derover, hvilket betyder, at børn kun kan få dette produkt, hvis en læge er villig til at ordinere det "off-label".
Guardian Connect mobilapp
På lanceringstidspunktet var denne gratis app kun tilgængelig for iOS-brugere. Men i maj 2020 meddelte Medtronic FDA-godkendelse af sin Android-version startende om sommeren. Det tilbyder nu også opdateringer til nogle ret seje udsættelses- og personaliseringsfunktioner til sporing og styring af blodsukker, som du kan læse om her.
Sugar.IQ mobilapp
Dette er en separat mobilapp, som Guardian Connect CGM-brugere også har eksklusiv adgang til. Det er den originale IBM Watson-app, som Medtronic købte og hypede, inden den til sidst lancerede den til et begrænset antal kunder, der brugte deres enkeltstående CGM i 2017.
Appen bruger IBM Watson-analyser til at finde mønstre i diabetesdata og tilbyder realtids, handlingsbar og personlig indsigt, som inkluderer en cirkulær graf, der afspejler time-in-range (TIR) data og en såkaldt "Glycemic Assist" til mad info. Medtronic har præsenteret videnskabelige data, der viser, at folk, der bruger Guardian Connect-systemet med Sugar.IQ-appen, oplevede 4,1 procent mere TIR sammenlignet med at bruge Guardian Connect alene - hvilket repræsenterer cirka en ekstra time om dagen. Derudover øgede de, der også brugte den valgfri glykæmiske hjælpefunktion til at gennemgå deres svar på specifikke fødevarer, TIR med yderligere 4 procent sammenlignet med dem, der ikke brugte denne funktion.

Fremtidige produkter under udvikling
Under ny ledelse siden oktober 2019 faldt Medtronic Diabetes-divisionen et par spændende detaljer om sin kommende tekniske pipeline, der skulle ind i den store American Diabetes Association (ADA) -konference i juni 2020:
Avanceret hybrid lukket sløjfe (780G)
Først forhåndsvist omkring ADA Scientific Sessions i juni 2019 vil virksomhedens 780G næste generations Advanced Hybrid Closed Loop (ACHL) system have den grundlæggende formfaktor for deres 6-serie insulinpumper. Det betyder et lodret "moderne" udseende sammenlignet med de ældre modeller med et vandret design, der ligner 1980'ernes personsøgere.

Nogle nøglefunktioner i 780G, vi har lært om:
- bruger en ny algoritme, som virksomheden siger er mere nøjagtig og pålidelig, udviklet som et resultat af partnerskabet med den israelske baserede DreaMed Diabetes, der blev annonceret i 2015.
- fungerer med den næste generation af Zeus CGM-sensor, som kun har 1 kalibrering den første dag og ikke kræver fingerstifter efter det.
- vil give automatisk korrektionsbolus hvert 5. minut for at hjælpe med at holde brugerne i et optimalt interval og automatisk justere for ubesvarede måltider.
- har et justerbart glukosemål mellem 100 og 120 mg / dL (sammenlignet med 670G's faste mål ved 120 mg / dL).
- tilbyder forskellige insulinvarighedstider i modsætning til andre tilgængelige kommercielle lukkede kredsløbssystemer.
- tilbyder indbygget Bluetooth, der er nødvendigt til datadeling og fjernovervågning, samt over-the-air fjernopdateringer til software, så brugerne ikke bliver forpligtet til at købe en helt ny enhed, hver gang nye funktioner lanceres. (I øjeblikket tilbyder kun Tandem t: slim X2 den mulige opdateringsfunktion).
- Medtronic planlægger at bede regulatorer om at OK dette nye system for voksne OG børn helt ned til 2 lige fra starten.
Ved ADA Sci-sessioner i juni 2020 frigav Medtronic vigtige nøgledata for dette kommende 780G-system, der viser bedre TIR-resultater og imponerende brugertilfredshedsmærker for systemets anvendelighed.
Dette system har nu godkendt CE-mærke i udlandet, og virksomheden er klar til at indgive 780G til FDA her i USA snart.
Bluetooth-tilsluttet 770G
Medtronic modtog FDA-godkendelse den 31. august 2020 for sin 770G, som er den BLE-aktiverede komponent i sin fremtidige 770G-enhed. Dette ses som et stopgap mellem den eksisterende 670G og den fremtidige 780G, der tilføjer Bluetooth-forbindelse til datadeling og fjernovervågning (noget konkurrerende enheder som Dexcom har tilbudt i årevis). Især er den tilgængelig for børn under 6 år og helt ned til 2 år.
Medtronic lancerer 770G først som en separat enhed inden den eventuelle frigivelse af den komplette 780G. Virksomheden bemærker, at kunder vil være i stand til nemt at opgradere til 780G og nyere funktioner eksternt, snarere end at kræve et nyt hardwarekøb (svarende til hvad Tandems tilbudte med sin fjernopdateringsfunktion i t: slim X2).
Udvidet slid infusionssæt
Medtronic præsenterede for nylig data om sit 7-dages infusionssæt, som kan bæres dobbelt så længe som aktuelle sæt, der er okay i maksimalt 3 dage. En amerikansk afgørende prøve er i gang, og dette nye infusionssæt er allerede godkendt i Europa.
I pressemeddelelser peger Medtronic på en ”ny og proprietær tilgang”, der adresserer insulinnedbrydning og konserveringstab - to ting, der kan resultere i okklusioner (insulin tilstopning i pumpeslanger) og dermed højere blodsukker. Sammen med opretholdelse af insulinstabilitet i de fulde 7 dage, vil den også bruge en ny klæbende teknologi til at hjælpe med at sikre, at den sidder fast på kroppen i den fulde slidtid.
Tidlige kliniske data viser, at personer, der bruger dette nye sæt, kan spare 5 til 10 hætteglas med insulin om året, der i øjeblikket spildes på grund af kravet om at ændre sættet hver 3. dag. Mindre hyppige indstillede ændringer ville også give mulighed for, at andre steder på huden kan hvile og helbrede, påpeger Medtronic.
Vi mindes dog om, at infusionssæt er blevet beskrevet som "akilleshælen" i moderne insulinpumpeteknologi, fordi de har mange svagheder. Medtronic har især ikke den mest succesrige track record på dette område. Husker du BD FlowSmart-teknologien, der blev lanceret som Medtronic Pro-sæt? Det varede ikke længe, da rapporter om knækkede kanyler førte til, at det oprindelige produkt blev trukket fra markedet af Medtronic. Virksomheden arbejdede sammen med BD for at undersøge problemerne og planlagde at genstarte dette infusionssæt, men til sidst skrottede BD konceptet fuldstændigt.
Fremtidige CGM-sensorer
Medtronic udvikler også sin næste generation af CGM-sensorer og styrker spillet fra dets originale Enlite-sensorer og den nuværende Guardian 3-version, der følger med Minimed 670G og stand-alone CGM. Virksomheden har antydet fremtidige CGM'er i årevis i videnskabelige præsentationer, men er ikke blevet drøftet offentligt meget indtil midten af 2020.

Indtil videre er de to nye modeller begge kendt af interne projektnavne, som sandsynligvis ikke vil være de endelige mærker:
- Project Zeus-sensor: ville stadig have et 7-dages slid og det samme muslingeskaldesign, men det ville være en "iCGM" -klassificering (FDA-godkendt til at integrere med andre enheder) og ville kun kræve fingerstikkalibreringer den første dag i brug.
- Project Synergy: en alt-i-en sensor / sender, der vil være fuldt engangs og få et nyt look. Med en fladere, firkantet formfaktor, der er 50 procent mindre end den nuværende model, vil den ikke kræve nogen overtape for at holde den på og vil have en enklere tretrins indsættelsesproces, der kun tager 10 sekunder. Det er usikkert, om det har en længere brugstid på 7 dage. Denne er sandsynligvis mindst et år eller to ud (~ 2022-23), da undersøgelsesstudier lige er begyndt.

Personlig lukket sløjfe
Medtronic arbejder allerede på denne fremtidige version af sit lukkede kredsløbssystem, der giver mulighed for endnu mere tilpasset kontrol via smartphone-interface - med optimering af autoindstillinger, valgfri automatisk carb-dækning og AI (kunstig intelligens), der lader det tilpasse sig patientens adfærd. Alle med et TIR-mål på 85 procent. En del af dette vil sandsynligvis omfatte Medtronic-opkøb af to startups, Nutrino Health og Klue, til måltidsbevægelsessporing og ernæringsdata-videnskab.
Det er altid et spørgsmål, hvornår noget overhovedet vil blive forelagt FDA, endsige faktisk godkendt, men i betragtning af FDA's banebrydende betegnelse, der blev tildelt denne undersøgelsesenhed i 2019, er det muligvis ikke for langt væk.
Doseringskrav (plus Medicare-dækning)
Medtronic har været langsom med at søge en "ikke-supplerende" status for deres CGM-sensorer, der ville eliminere kravet om fingeraftrykbekræftelser og give mulighed for Medicare-dækning. Mens hver anden CGM-konkurrent har fanget denne FDA-betegnelse, har Medtronic trukket fødderne for at forfølge den.
Alligevel fortæller virksomheden DiabetesMine, at det havde haft det i tankerne i en årrække og planlægger at forfølge det til deres Guardian 3-sensor og 780G-systemet inden længe. Hvis de godkendes af regulatorer, vil det tillade, at virksomhedens enkeltstående Guardian 3 CGM-system såvel som de sensorudvidede enheder er berettiget til Medicare-dækning.
Tubeless patch pumpe?
Der var engang Medtronic Diabetes syn på en patchpumpe, der ikke ville omfatte den traditionelle slange, som dens enheder havde. Industriobservatører husker virksomhedens plan tilbage i 2008 - kun få korte år efter, at den rørløse Omnipod først kom på markedet - om at udvikle sin egen engangspatchpumpe.
Medtronic Diabetes skrabede alt sammen den idé for mange år siden, men så ofte får den en omtale og fornyet interesse. Fra midten af 2020 er Omnipod den eneste i sin slags på trods af mange patch-pumpe-wannabes, der er kommet og gået og stadig taler om fremtidige produkter.
Interoperabilitetsvej
Som en del af al denne fremtidige teknologi, løber Medtronic op til vigtige forsøg, der er nødvendige for at få den eftertragtede "iCGM" interoperabilitetsklassifikation. Fra midten af 2020 har Dexcom G6 denne betegnelse til at arbejde med lukket kredsløbsteknologi, mens FreeStyle Libre 2 har en begrænset version af iCGM-status, hvilket betyder, at den i øjeblikket ikke kan bruges med automatiserede insulinafgivelsesenheder.
I juni 2019 meddelte Medtronic og Tidepool, at de ville arbejde på et fremtidigt interoperabelt lukket kredsløb - adskilt fra de ovennævnte 780G / AHCL- og personaliserede lukkede loop-systemer. Intet ord om, hvor langt det kan være, og hvilke funktioner det kan tilbyde.
Udgået teknologi
Vi så endelig slutningen på en æra med Medtronic's originale insulinpumpemodeller, der lignede farverige personsøgere i 2018. Disse er stadig meget udbredte, men er nu officielt ophørt og ikke længere tilgængelige for køb. Forsyningerne bliver sværere at finde, når tiden bevæger sig fremad.

I sin storhedstid var Minimed 530 monumental, fordi den gjorde, som ingen anden insulinpumpe havde gjort før: Den suspenderede automatisk levering af insulin, hvis du krydsede en bestemt lav glukosetærskel. Medtronic fik FDA-godkendelse for den lavsukkersuspenderings- (LGS) eller tærskelsuspenderingsfunktion i september 2013, og den forblev tilgængelig indtil oktober 2018, da Medtronic ophørte med den og tidligere pumper i "5-serien" til fordel for de nyere enheder i 6-serien.
Ironisk nok bruger mange i #WeAreNotWaiting DIY (gør-det-selv) diabetes-innovationssamfundet stadig disse ældre insulinpumpemodeller, da de forbliver ret pålidelige og - dækker dine ører, FDA og diabetespædagoger er glade for off-label produktbrug - er i stand til at blive hacket.
På trods af en FDA-advarsel og almindelig medie bekymring i 2019 om, at disse hjemmelavede systemer ikke er cybersikre på grund af den forældede teknologi, forbliver de i omløb.
Adgang til diabetes betyder noget
Adgang og overkommelighed er kritiske spørgsmål, der findes som barrierer for teknologi for for mange inden for diabetesfællesskabet.
Forsikringsdækning spiller en stor del af det, men desværre har Medtronic været et kontroversielt selskab på den front i de senere år.
I sit skub mod "værdibaseret" eller "resultatorienteret" pleje underskrev Medtronic i 2016 en aftale med sundhedsforsikringsgiganten United Health Care (UHC), der gjorde Medtronic's pumper til det "foretrukne brand" for sine planholdere. En lignende aftale blev fulgt i 2019 for den nyeste Medtronic-teknologi, der er godkendt til børn.
Denne valgbegrænsning gned mange i D-samfundet den forkerte måde, for at sige det mildt. Mens UHC og Medtronic begge påpeger, at der i visse tilfælde kan gøres undtagelser, raser kampen mod denne form for ikke-medicinsk skift, der tilsidesætter læge- og patientpræferencer af forretningsmæssige årsager. Heldigvis begyndte UHC at tilbyde et valg den 1. juli 2020, da det udvidede de varemærkebeskyttede varer til at omfatte Tandem Diabetes-teknologi sammen med Medtronics produkter.
I sidste ende kommer det ned til den enkle virkelighed, som #DiabetesAccessMatters. Ingen forminnovation har betydning, hvis folk ikke kan få fat i det.
Mens Medtronic helt sikkert fortjener kredit for, hvad det har opnået med at bringe ny teknologi til samfundet, beder vi dem om at hjælpe med at fremme patientens og lægenes valg.


-supplies-at-the-pharmacy.jpg)