For opdateret dækning af diabetesteknologielandskabet her er et kig på, hvad man kan forvente i 2021.

Ankomsten af et nyt år bringer altid øget håb om nye fremskridt inden for diabetesværktøjer og pleje. I år er teknologispektrationerne særligt høje, da vi er ved at se et boom i lukkede kredsløbssystemer, der delvist automatiserer insulinafgivelse (aka Artificial Pancreas tech).
Vores team i 'Mine har lyttet til indkomstopkald fra industrien, talt med virksomhedens insidere og generelt "læst tebladene" om, hvad der er i horisonten. Her er en oversigt over, hvad vi forventer at se realisere sig inden for diabetesteknologi i 2020, med nogle af vores egne indsigter og observationer sprinklet ind i:
Tandem diabetesbehandling
Control-IQ: FDA-godkendelse af denne nye teknologi fra Tandem var den store historie ved årets udgang for 2019. Control-IQ bliver det mest avancerede kommercielle lukkede kredsløbssystem til rådighed. Tandem vil udrulle den fra midten af januar 2020 sammen med en ny mobilapp, der muliggør automatisk upload af diabetesenhedsdata til dens t: connect-webplatform. Vi får at vide, at nye funktioner til den mobile app gradvist vil blive afsløret fra midten af 2020, herunder datavisning og integration af andre sundhedsdata; i sidste ende vil de tilbyde fuld mobiltelefonstyring af t: slim X2 insulinpumpe via appen! Se vores fulde dækning af Control-IQ her.
t: sport mini-pumpe: 2020 kan også medbringe en ny Tandem mini pumpe kaldet "t: sport." Det vil være en slags slags hybrid, omtrent halvdelen af størrelsen på t: slank X2-pumpe og slet uden nogen skærm. Især ville det være den første patch-pumpe-stilmulighed ud over Omnipod og inkluderer en sideknap til en hurtig insulindosis fra selve enheden. T: sporten vil have en klæbende del til din krop-klæbende del på bagsiden, men løsner og også t: slim's varemærke pigtail-insulinrør, der fastgøres til infusionssættet til insulinafgivelse. Nu da Control-IQ er godkendt og lanceret, skubber Tandem fremad med at indgive t: sport til FDA-gennemgang i midten af 2020. Håbet er at give kunderne et valg af, hvordan de vil bruge det: enten via smartphone-app eller en separat modtager. Den første FDA-arkivering midt på året vil være centreret om den håndholdte modtager, mens en senere 2020-arkivering vil fokusere på mobilappens kontrol af enheden. Alt dette afhænger af FDAs beslutningstagning, men vi er optimistiske i betragtning af Tandems succes med at få Control-IQ ud af døren.
Insulets Omnipod
Omnipod Horizon Closed Loop: Håber du på en kommerciel version af et lukket kredsløbssystem med en patchpumpe? Dette kan meget vel være året for Insulet Corp. at lancere sit officielle lukkede system kaldet Omnipod Horizon.
I 2019 lancerede insulinplastpumpefirmaet sin forløber Omnipod DASH-version, og vi så også en gør-det-selv-version af Loop dukke op, der er kompatibel med Omnipod-rørløse pumpe. Vi er glade for at se en "officiel" version af dette system med potentiel smartphone-mobilapp-kontrol forhåbentlig kommer snart i år. Insulet siger, at det forventer at indgive midt i året med en håbefuld godkendelse og begrænset lancering inden udgangen af 2020 og en fuld kommerciel lancering i 2021.
Medtronic Diabetes lukket sløjfe
Advanced Hybrid Closed Loop (AHCL eller 780G): Annonceret omkring ADA Scientific Sessions i juni 2019 vil dette næste generations “Advanced Hybrid Closed Loop (ACHL) system” have den grundlæggende formfaktor for virksomhedens 6-serie modeller med en lodret “moderne” udseende sammenlignet med de ældre modeller med et vandret design, der lignede personsøgere fra 1980'erne.
780G bruger en ny algoritme, som virksomheden siger er mere præcis og pålidelig. Det vil give automatisk korrektion bolusing, vil automatisk justere for ubesvarede måltider og tillade et justerbart glukosemål ned til 100 mg / dL (sammenlignet med 670G's indstillede mål ved 120 mg / dL). Det sigter også mod at opnå 80% brugertid inden for rækkevidde sammenlignet med den eksisterende 71% TIR vist i data på 670G.
Det er vigtigt, at denne BLE-aktiverede pumpe-CGM-kombination muliggør opdatering af ekstern software - som det tilbydes af Tandems t: slim X2 - så brugerne bliver ikke forpligtet til at købe en helt ny enhed, hver gang nye funktioner lanceres. Det vil også have den indbyggede BLE, der er nødvendig for datadeling-forbindelse. Medtronic siger, at de allerede har sendt den BLE-tilsluttede komponent af denne enhed til FDA. Kliniske forsøg er i gang (se her og her) og skulle indgå i midten af 2020. Virksomhedens oprindelige mål for april 2020 ser ud til at være alt for ambitiøst, da 780G-afprøvningen ikke forventes afsluttet før midt i året. Stadig, hvis Medtronic arkiverer denne enhed, kunne vi se den starte i slutningen af 2020.
Bemærk også: Tidligere havde Medtronic oplyst, at de havde planer om at lancere en BLE-aktiveret version af 670G, der muliggør fjerndeling og datavisning via mobilapp. Men MedT har nu sagt, at de ikke længere planlægger den tilsluttede 670G-version og i stedet vil fokusere på at bringe 780G med indbygget BLE på markedet ASAP.
Abbott Diabetes Care
Libre 2.0: Vi venter stadig på denne, efter at virksomheden sendte den til regulatorer i starten af sidste år. Denne næste generations version af FreeStyle Libre Flash Glucose Monitoring (FGM) -systemet inkluderer en lille rund diskstørrelsessensor, der bæres på armen, som du scanner med en modtager for at få glukoseaflæsninger. Libre 2.0 vil medbringe valgfri alarmer via Bluetooth Low Energy (BLE), der alarmerer, hvis du er uden for rækkevidde, for at bede dig om at foretage en fingerstick-kontrol for at bekræfte en faktisk lav eller høj aflæsning.
Vi har hørt, at FDA har overvejet, om denne enhed skal tildeles den nye "iCGM" -betegnelse, der vil betragte den som officielt interoperabel med andre sådanne enheder, som Tandem t: slim X2. Så mens vi håber på 2020, er det muligt, at FDA ikke vil være fortrolig med at give Libre 2.0 iCGM-mærket, da enheden ikke automatisk advarer med en faktisk glukoseaflæsning, som andre iCGM-enheder gør.
Dexcom CGM
Dexcom målretter mod en indledende lancering af sin næste generation G7-model i slutningen af 2020, som har været i værk i flere år som et samarbejde med Verily (tidligere Google Life Sciences). Mens detaljerne stadig er ringe, antydede Dexcom's nogle store revisioner af, hvad G7 vil tilbyde:
Forlænget slid på 14-15 dage: Dette tilføjer yderligere fire til fem dage sammenlignet med det nuværende 10-dages slid på Dexcom G6. Som med G6 er der ikke behov for kalibreringer af fingerstikker.
Fuldt engangsbrug: I modsætning til Dexcom CGM-modeller til dato vil G7 være fuldt engangsbrug, så du har ikke en separat sender med en batterilevetid på tre måneder. I stedet for vil sensoren og senderen være fuldt integreret, og når sensorens kørsel er færdig, bortskaffer du hele den integrerede enhed.
Tyndere: Dexcom siger, at G7 vil være den tyndeste generation af sine CGM-sensorer endnu, men virksomheden har ikke frigivet nogen specifik detalje om målinger eller design.
Beslutningsstøtte: Selvom vi endnu ikke har set dette integreret i eksisterende G6-teknologi, er det stadig muligt og vil sandsynligvis blive flettet ind i den fremtidige G7. Dexcom har talt om dette før om at øge udvidelsen af CGM til flere type 2'er såvel som ud over dem med diabetes. I betragtning af Dexcoms erhvervelse af TypeZero, og hvordan det nu er internt, er det grund til at se, at flere softwarefunktioner som doseringshjælp og interaktion er inkluderet i Dexcom CGM-tilbudene, når vi bevæger os fremad.
Dexcom har endnu ikke indgivet G7 til FDA, men i forbindelse med indtjeningen i 3. kvartal i november 2019 siger de, at de planlægger en begrænset lancering i slutningen af 2020 efterfulgt af en mere bred kommerciel lancering i 2021. Det californiske selskab har været øger sin produktionskapacitet det sidste år med G6 og siger, at det baner vejen for en jævn lancering af sit næste generations produkt.
Selvfølgelig arbejder virksomheden også med at løse serverudfaldsproblemerne, der opstod to gange i 2019 - en gang over nytårsferien 2018-2019 og en længere strækning over Thanksgiving 2019-weekenden. CEO Kevin Sayer udsendte en YouTube-undskyldning for dette mod årets slutning og noterede sig specifikt, at ingeniører fremskynder en plan for implementering af underretninger i appen i tilfælde af eventuelle datadeling i fremtiden. Dexcom siger, at det også planlægger at opdatere virksomhedswebstedet med en destinationsside, der viser 24/7 opdateringer af systemfunktionalitet.
Implantabel CGM fra Eversense
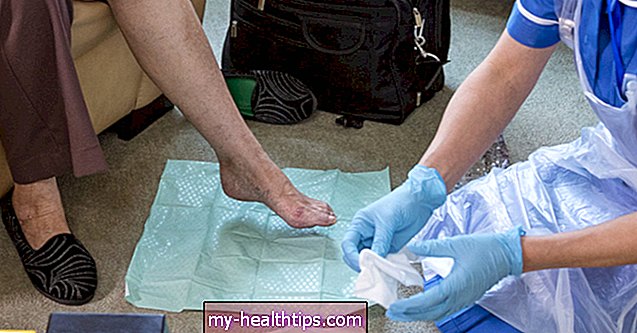
Mobile App: Fra slutningen af 2019 har denne 90-dages implanterbare CGM fra Senseonics nu et "doseringskrav" fra FDA - hvilket betyder, at det sammen med Abbott Libre og Dexcom ikke kræver kalibreringer af fingerstikker for at bekræfte aflæsninger inden dosering af insulin eller tilberedning andre behandlingsbeslutninger. Mærkeligt nok kræver virksomhedens nye mobilapp to kalibreringer om dagen for at sikre kontinuerlig nøjagtighed i løbet af 90-dages sensorlevetid, men "den nye app giver også fleksibilitet med dine kalibreringstider," siger Senseonics.
Længere slid: Vi venter på meddelelse om tilgængelighed i USA af en 180-dages sensor med længere slid (tilgængelig uden for USA som Eversense XL). Det betyder, at brugerne kun behøver at få det implanteret og udskiftet hver sjette måned sammenlignet med hver tredje måned, som det i øjeblikket er tilfældet. Senseonics siger, at de snart forventer godkendelse fra lovgivningen med en forventet lancering i 2020.
Bluetooth-forbindelse til Afrezza
Hej, BluHale! MannKind Corp., producenter af Afrezza inhaleret insulin, fortæller os, at de vil lancere en BluHale Pro i 2020 specielt til sundhedsudbydere. Denne tilføjelsesadapter gør det muligt for Afrezza inhalatorenheden at have forbindelse.
Selvom det først ikke inkluderer doseringsdata, overvåger BluHale Pro inhalationsteknik, som læger kan bruge til at træne nye patienter. Enheden er kompatibel med Android-, iPhone- og Microsoft-enheder. Det blinker et grønt lys, hvis Afrezza inhaleres ordentligt og et rødt lys, hvis ikke. Læger kan se de sporede data om disse tilfælde og derefter tilbyde deres patienter råd om, hvordan de bedst kan bruge Afrezza. BluHale vil i sidste ende også være i stand til at spore og dele doseringsdata.
MannKinds administrerende direktør Michael Castagna siger, at de også planlægger at starte deres fase 3-pædiatriske forsøg snart, hvilket er det sidste skridt, før de fortsætter lovgivningsmæssigt OK for Afrezza-brug hos børn.
Xeris Glucagon-pen
Gvoke HypoPen: I efteråret 2019 fik Xeris, der er baseret i Chicago, FDA-godkendelse for verdens første klar til brug stabile flydende glukagon-nødpen, som en EpiPen til redning af diabetes. Men virksomheden valgte først at lancere sin forudfyldte injektionssprøjte før HypoPen til engangsbrug - som nu forventes i juli 2020.
Den efterlængte version af autoinjektoren indeholder en 6 mm nål, men du kan aldrig se nålen, da pennen er uafhængig til hurtig engangsbrug og bortskaffelse. I skarp kontrast til eksisterende glucagon-sæt er det en nem totrinsproces at bruge: Træk bare den røde hætte af og skub Gvoke HypoPen ned på huden i fem sekunder, indtil vinduet bliver rødt. Det er det! Derefter trækker pennen automatisk tilbage og låses, så den ikke kan bruges igen. Den ikke-forsikringsmæssige kontantpris er $ 280 pr. Injektor, den samme som den fyldte sprøjte.
Lilly Connected Pens og mere
Ny tilsluttet pen: I december 2019 godkendte FDA Lillys forudfyldte engangs insulinpen beregnet til at være grundlaget for deres nye penbaserede tilsluttede digitale platform. Virksomheden siger, at det arbejder tæt sammen med FDA for at bestemme lovgivningsmæssige krav til yderligere komponenter på platformen, herunder vedhæftet fil, der overfører insulindoseringsdata fra pennen til en mobilapp. Til sidst fungerer dette med Dexcom CGM (kontinuerlig glukosemonitor), da de to virksomheder netop har underskrevet en aftale med det formål. Det hele vil blive lanceret sammen, når FDA godkender den tilsluttede penplatform.
Lilly fortæller os også, at på den kommende ATTD-konference, der finder sted i Madrid i slutningen af februar, vil de præsentere forskning om "en potentiel mobilapp, der vil give personlig proaktiv vejledning ... omkring træning." Det vil være en del af deres "større Connected Care-program."
Ultra-Rapid Lispro Insulin (uRLi): Dette er et nyt endnu hurtigere virkende måltidsinsulin. Nylige kliniske data viser, at uRLi klokket ind efter 13 minutter sammenlignet med Humalog og andre måltider, der tog så lang tid som 27 minutter at begynde at påvirke glukoseniveauerne. Det reducerede også spidser efter måltid mere dramatisk. Lilly indsendte URLi til regulatorer i USA såvel som Europa og Japan i løbet af 2019, og Pharma-giganten forventer godkendelse fra lovgivningen på alle tre markeder i 2020.
Ny hybridpatchpumpe: Lillys hybrid lukkede loop-system er stadig under udvikling, og virksomheden planlægger snart at præsentere data om tidlige gennemførlighedsdata om det. Selvom vi ikke forventer at se dette lanceret i 2020, forventer vi at høre opdateringer om udvikling og tidlige forsøg.
Kommer også lidt senere ...
WaveForm Cascade CGM: WaveForm Technologies er en spin-off af enhedsselskabet AgaMatrix, og de udvikler en ny CGM, der vil blive indgivet til FDA i 2020, men det forventes ikke at være tilgængelig i år.
Enheden, der fik CE-mærket godkendelse i november 2019, er en 14-dages CGM-sensor med en genopladelig firkantet sender, der kommunikerer til både Android- og iOS-mobilapps via Bluetooth. På et nylig møde med Diabetes Technology Society viste virksomheden en videnskabelig plakat, der viser konceptuelle billeder og nøjagtighedsdata. På 11,9% MARD er det ikke så godt som eksisterende CGM'er, men på niveau med de fleste førstegener-iterationer. Amerikanske kliniske undersøgelser og oversøisk lancering forventes i 2020, og WaveForm fortæller os, at de planlægger en lancering i 2021 her i USA.
BD Patch Pump til T2: Vi har også ventet i flere år på denne nye fuldt engangs, tre-dages slangepumpe fra Pharma-gigant BD. Det vil tilbyde både basal- og bolusdosering, rummer 300 enheder og har en genanvendelig håndholdt controller med Bluetooth-forbindelse til en smartphone-app.
BD har talt om, at det meget enkle pumpedesign er mere sammenligneligt med insulininjektionsbehandling for mennesker med type 2-diabetes, hvilket gør det potentielt til en bedre mulighed for dem, hvis forsikringsselskaber vil modstå at godkende en komplet traditionel insulinpumpe. I et indtjeningsopkald i august 2019 meddelte BD, at de havde trukket sin FDA-ansøgning om dette produkt tilbage, men den daværende administrerende direktør Victor Forlenza (som blev udskiftet i september 2019) understregede stadig, at BD arbejdede på det med en tredjeparts F & U-partner og "forblev engageret" til patchpumpen.
Tidepool Loop: Den gratis software og open source-data non-profit Tidepool bygger et lukket kredsløbssystem, der samler både DIY-verdenen og FDA-reguleret kommerciel side. Selvom det vil være baseret på DIY Loop hjemmelavede systemer, fungerer denne separate Tidepool Loop-mobilapp med Dexcom CGM og Omnipod slangeløs patchpumpe og er tilgængelig på iOS oprindeligt. Vi får at vide, at organisationen arbejder med tilsynsmyndigheder og forsker i kliniske forsøg i første halvdel af 2020 og planlægger at indgive en ansøgning til FDA inden årets udgang. (FYI: Tidepool opdaterer sine fremskridt på organisationens blog, så hold også øje med det.)
Bigfoot Biomedical: Spænding er fortsat omkring denne # WeAreNotWaiting græsrodsfødte lukket sløjfe-teknologi, men planerne er lidt anderledes, end de var for et år siden. Starten fortsætter med at bruge basisdesignet fra den tidligere Asante Snap insulinpumpe til deres hovedprodukt kaldet Bigfoot Autonomy, men før det håber vi stadig at se fremskridt i 2020 med den tilsluttede penversion med navnet Bigfoot Unity. Ved vores nylige DiabetesMine University-begivenhed i november satte administrerende direktør Jeffrey Brewer en tidslinje fra 2021 til det første generations Unity-produkt med en næste generations version året efter. Selvom vi for nylig hører Bigfoot planer om at indgive Unity-penversionen i slutningen af 2020 med en mulig lancering, der er planlagt til slutningen af året, så vi skal se. Det Autonomy-pumpebaserede system er planlagt til at følge, muligvis i 2023.
Beta Bionics iLet: Mange er begejstrede for "FDA's gennembrudte enhedsbetegnelse" modtaget af dette lukkede sløjfe-tech-firma i december 2019, men vi er stadig mindst et år eller to væk fra at se dette produkt klar til lancering. Vi forventer, at der kun er en insulinversion, inden vi til sidst kommer til versionen med dobbelthormon med både insulin og glukagon inde i pumpen. Se 2019 DiabetesMine University forhåndsvisning af Beta Bionics-systemet her.
Selvfølgelig betyder alle ovenstående innovationer intet, hvis folk ikke har råd til eller får fat i dem. Vi ser heldigvis stigende fremskridt med hensyn til overkommelige priser, men har stadig en lang vej at gå i 2020 og derefter.
Vi i 'Minen kalder os selv "skeptiske optimister", så vi håber, at dette år kan bringe meningsfulde fremskridt, der er tilgængelige for så mange PWD'er som muligt.
Meget ændret sig i 2020 på grund af den globale sundhedspandemi, så sørg for at læse vores opdaterede DiabetesMine-dækning om diabetesteknologi forventet i 2021.